Возможности ТРУЗИ с ультразвуковой ангиографией в оценке местного распространения рака предстательной железы
Рубрика: Эхография в урологии
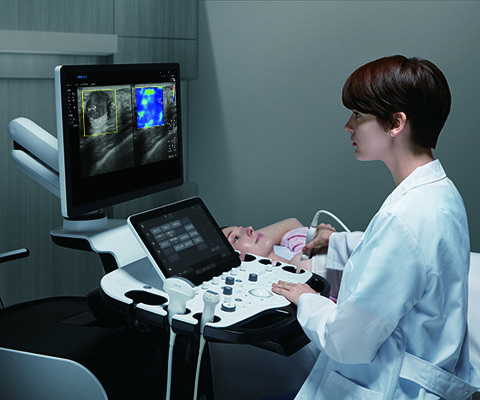
УЗ сканер Samsung RS85
Аппарат премиум класса со встроенным искусственным интеллектом, для лечебных учреждений с высокими требованиями к ультразвуковой диагностике.
Введение
В настоящее время проблема диагностики рака предстательной железы (РПЖ) актуальна в связи с неуклонным ростом заболеваемости и смертности. Рак предстательной железы - самое частое злокачественное заболевание среди мужской группы населения [2-4, 11, 13]. Ежегодно в мире выявляется до 396 тыс. случаев [1]. В структуре онкологической заболеваемости у мужчин рак предстательной железы продолжает занимать лидирующее место, составляя 13 % в экономически развитых странах Европы и США [3]. В России рак предстательной железы составляет 10,9-11,3 случаев на 100 тыс. населения [7]. Учитывая, что пик заболеваемости приходится на шестое-седьмое десятилетия жизни, а демографическая обстановка характеризуется устойчивой тенденцией к увеличению числа лиц пожилого возраста, эпидемиологический прогноз предсказывает дальнейший рост больных раком предстательной железы [13]. Ожидается, что к 2007 г. число больных раком предстательной железы составит 1,6 млн человек, ежегодный рост заболеваемости - 3,8 % [3, 5].
При первичном обращении метастазы выявляют у 60-80% больных [6, 9]. В течение первого года с момента установления диагноза рак предстательной железы умирают 20,1 % больных [3]. У пациентов более молодого возраста отмечается тенденция к более злокачественному течению с развитием низкодифференцированных форм и низким уровнем 5-летней выживаемости [3]. В этой связи существует настоятельная необходимость в разработке и применении методов, которые могли бы обеспечить раннее выявление заболевания и оценить распространенность опухолевого процесса для выбора оптимальной тактики лечения.
В настоящее время трансректальное ультразвуковое исследование (ТРУЗИ) получило широкое распространение как наиболее экономичный, простой и в то же время достоверный скрининговый метод визуализации предстательной железы, благодаря высокой информативности, неинвазивности, отсутствию лучевой нагрузки, возможности многократного повторения [6, 8, 12]. С появлением и совершенствованием более информативных методов лучевой диагностики, таких как компьютерная и магнитно-резонансная томография (КТ и МРТ), их по праву считают приоритетными в диагностике местного распространения и наличия отдаленного метастазирования при раке предстательной железы [6, 10]. В ряде случаев клиницисты "забывают" о возможностях традиционного ультразвукового исследования, и при обследовании пациентов единственными являются КТ и МРТ.
Диагностические возможности ТРУЗИ в выявлении рака предстательной железы были оценены в большом количестве работ [5, 6, 8], однако его совместное использование с ультразвуковой ангиографией в оценке местного распространения рака предстательной железы освещено недостаточно.
В нашей работе мы попытались сопоставить информативность ТРУЗИ в сочетании с ультразвуковой ангиографией и МРТ в диагностике первичного очага и местного распространения рака предстательной железы.
Материалы и методы
Обследовано 65 пациентов, страдающих раком предстательной железы (возраст 51-82 года, средний возраст - 65,6±8,82 года). Диагноз всех пациентов подтвержден данными комплексного обследования на поликлиническом и стационарном этапах, которое включало анамнез, клинические и лабораторные исследования, анализ гистологического материала, полученного после оперативного вмешательства или после проведенных под контролем ТРУЗИ пункционных биопсий, а также результатами нескольких визуальных методов исследования.
Всем пациентам было проведено ТРУЗИ на аппаратах экспертного класса, оснащенных режимами цветового и энергетического допплеровского картирования, трехмерной ангиографией, и магнитно-резонансная томография органов малого таза - на томографе "Magnetom Harmony", фирмы "Siemens" с напряженностью магнитного поля 1Т (с получением сагиттальных Т2-взвешенных изображений; аксиальных Т1- и Т2-взвешенных изображений, в том числе с подавлением сигнала от жировой ткани; коронарных Т2-взвешенных изображений).
При ТРУЗИ в режиме серой шкалы проводилась оценка: объема, структуры и эхогенности участков опухоли, состояния прилежащих к ним капсул железы и(или) хирургической капсулы, а также исследовались состояние, диаметр и структура семенных пузырьков; толщина и эхоструктура прилежащей стенки прямой кишки и задней стенки мочевого пузыря.
При ТРУЗИ с ультразвуковой ангиографией оценивали симметричность сосудистого рисунка железы; ход сосудов, степень васкуляризации железы и участков опухоли; прилежащих проксимальных отделов семенных пузырьков, степень васкуляризации стенки прямой кишки и задней стенки мочевого пузыря.
При МРТ осуществлялась оценка размеров предстательной железы с использованием сагиттальных и поперечных изображений, оценка внутренней зональной анатомии железы, латеральных границ простаты, передних и латеральных венозных сплетений и семенных пузырьков; при выявлении зон измененной интенсивности сигнала оценивались их локализация, характеристика данной зоны, а также взаимоотношение с другими структурами предстательной железы. Определялось распространение процесса на костные структуры таза, пояснично-крестцового отдела позвоночника, регионарные лимфатические узлы. Данные ТРУЗИ сопоставлялись с клиническими, лабораторными результатами и МРТ.
Результаты
При исследовании значения уровня общего ПСА его повышение более 4 нг/мл отмечалось у 60 (92%) пациентов, у остальных (8%) - значение общего ПСА было в пределах 0-4 нг/мл. По данным ТРУЗИ, в режиме серой шкалы у большинства пациентов объем железы был умеренно увеличен и в среднем составлял 43,5±5,2 см³ ( от 15,05 до 151,2 см³).
При ТРУЗИ, включавшем в себя как исследование в В-режиме, так и использование методик ультразвуковой ангиографии, было выявлено 103 участка измененной эхоструктуры, эхогенности или васкуляризации паренхимы предстательной железы, которые на основании характеристик и результатов лабораторных данных были расценены как опухоли. По данным МРТ было выявлено 89 участков (табл. 1).
| Признак | Абсолютное значение (%) | |
|---|---|---|
| ТРУЗИ | МРТ | |
| Контуры участка: | ||
| четкие | 16 (15,5) | 5 (5,6) |
| нечеткие | 87 (84,5) | 84 (94,4) |
| ровные | 8 (7,8) | 6 (6,70) |
| неровные | 95 (92,2) | 83 (93,3) |
| Характеристика эхогенности / интенсивности участка: | ||
| гипоэхогенного | 78 (75,7) | 79 (88,8) |
| сниженной эхогенности | 14 (13,6) | — |
| изоэхогенного с измененной структурой | 7 (6,8) | 5 (5,6) |
| смешанной эхогенности / интенсивности | 4 (3,9) | 5 (5,6) |
| Структура участка: | ||
| однородная | 47 (45,6) | 51 (57,3) |
| неоднородная | 56 (54,4) | 38 (42,7) |
| Объем опухоли, см³: | ||
| 0,42-2,5 | 13 | 12,6 |
| 2,6-5,5 | 38 | 36,9 |
| 5,6-10,5 | 35 | 33,9 |
| 10,6-15,5 | 9 | 8,7 |
| 15,6-20,5 | 5 | 4,9 |
| 20,6-35,5 | 3 | 2,9 |
При ТРУЗИ с УЗ-ангиографией производилась качественная и количественная оценка васкуляризации выявленных участков опухоли у пациентов с раком предстательной железы, распределения сосудистого рисунка в опухолевом участке, симметричность сосудистого рисунка паренхимы ПЖ.
В результате проведенных исследований было определено, что в 64 (62,1%) случаях участки были гиперваскулярны по сравнению с контралатеральным неизмененным участком паренхимы железы, в 26 (25,2%) случаях определялись гиповаскулярные участки. В 13 (12,6%) участках опухоли количество сосудов было сопоставимо с количеством сосудов, определявшихся в контралатеральном участке ПЖ. Во всех участках отмечалась деформация сосудистого рисунка.
При экстракапсулярном распространении оценивались состояние капсулы железы и хирургической капсулы в проекции участка опухоли, состояние семенных пузырьков со стороны опухоли, а также толщина и эхоструктура прилежащей стенки прямой кишки и задней стенки мочевого пузыря (табл. 2).
| Наименование | ТРУЗИ - B-режим, режим ультразвуковой ангиографии (%) | МРТ (%) |
|---|---|---|
| Собственная капсула: | ||
| прослеживается | 61 (59,2) | 54 (60,7) |
| фрагментарна | 26 (25,2) | 15 16,8) |
| не прослеживается | 16 (15,5) | 20 (22,4) |
| Хирургическая капсула: | ||
| прослеживается | 79 (76,7) | 58 (65,2) |
| фрагментарна | 18 (17,5) | 14 (15,7) |
| не прослеживается | 6 (5,8) | 17 (19,1) |
| Семенные пузырьки: | ||
| вовлечены | 21 (20,4) | 29 (32,6) |
| не вовлечены | 82 (79,6) | 60 (67,4) |
| Перипростатическая клетчатка: | ||
| вовлечена | 49 (47,6) | 52 (58,4) |
| не вовлечена | 54 (52,4) | 37 (41,6) |
| Параректальная клетчатка: | ||
| вовлечена | 41 (39,8) | 39 (43,8) |
| не вовлечена | 61 (60,2) | 50 (56,2) |
| Стенка прямой кишки: | ||
| вовлечена | 19 (18,4) | 17 (19,1) |
| не вовлечена | 84 (81,6) | 72 (80,9) |
| Задняя стенка мочевого пузыря: | ||
| вовлечена | 4 (3,9) | 7 (7,9) |
| не вовлечена | 99 (96,1) | 81 (92,1) |
Из табл. 2 следует, что данные ТРУЗИ были сопоставимы с данными МРТ при оценке: собственной капсулы железы, перипростатической и параректальной клетчатки и стенки прямой кишки. МРТ была более информативна при выявлении распространения опухолевого процесса на семенные пузырьки, заднюю стенку прямой кишки и в визуализации хирургической капсулы предстательной железы.
Клиническое наблюдение
Пациент П., 1923 г.р., рак предстательной железы с экстракапсулярным распространением процесса на область перипростатической клетчатки, семенные пузырьки и метастатическим поражением позвоночника. При этом отмечались: асимметричное расширение семенного пузырька со стороны поражения, нечеткая дифференцировка между проксимальным отделом семенного пузырька и паренхимой железы, нечеткость контуров пузырька, наличие неоднородного содержимого. В случае двустороннего вовлечения семенных пузырьков в процесс увеличение их диаметра будет двусторонним. При ультразвуковой ангиографии на границе паренхимы железы и измененного семенного пузырька определялась гиперваскуляризация и деформация сосудистого рисунка (рис. 1 а-г). Трехмерная ангиография позволяет более полно визуализировать сосудистый рисунок железы.

а) В-режим. Изоэхогенный участок опухоли неоднородной структуры (маркеры). Капсула железы над ним выбухает, не прослеживается. Дифференцировка на зоны слева отсутствует, справа хирургическая капсула приподнята, визуализируется фрагментарно.

б) Режим энергетического допплера и трехмерной реконструкции сосудистого рисунка в этом же режиме - гиперваскуляризация и выраженная деформация сосудистого рисунка.

в) Режим энергетического допплера и трехмерной реконструкции сосудистого рисунка в этом же режиме - гиперваскуляризация и выраженная деформация сосудистого рисунка.

г) В-режим. Капсула железы над участком в проекции срединной бороздки приподнята, нечетко дифференцируется от стенки прямой кишки. В данной проекцииона несколько утолщена, эхогенность ее снижена.
При распространении опухоли на стенку прямой кишки и(или) заднюю стенку мочевого пузыря в В-режиме отмечалась нечеткая дифференцировка (или ее отсутствие) между паренхимой железы и неравномерно утолщенными стенкой прямой кишки и(или) задней стенкой мочевого пузыря, наблюдалась асимметрия формы мочевого пузыря, асимметрия контуров железы в проекции данной зоны, ригидность железы при надавливании датчиком (при распространении опухоли на стенку прямой кишки). При ультразвуковой ангиографии в подкапсульных отделах железы и утолщенных стенке прямой кишки и(или) стенке мочевого пузыря визуализировалась гиперваскуляризация с наличием общих деформированных сосудов (рис. 2 а-в).

а) В-режим. Семенные пузырьки асимметричные.

б) В-режим. Правый семенной пузырек дифференцируется четко от паренхимы железы, не расширен, структура его умеренно неоднородная, контуры его четкие.

в) Режим энергетического допплера. При ультразвуковой ангиографии в базальных отделах предстательной железы и в проксимальном отделе левого семенного пузырька выраженная гиперваскуляризация и деформация сосудистого рисунка.
При МРТ исследовании в аксиальном Т2-взвешенном изображении, импульсной последовательности (ИП) TSE выявлено: в периферической зоне железы слева, с распространением на центральную зону слева определяется участок опухоли со сниженной интенсивностью сигнала, распространяющийся за пределы железы на перипростатическую клетчатку. Капсула железы над данным участком не прослеживается. Обращает на себя внимание наличие очагов сниженной интенсивности сигнала в костях таза и правой бедренной кости - метастатическое поражение (рис. 3 а); при аксиальном Т1-взвешенном изображении, ИП TSE - участок опухоли изоинтенсивен в периферической зоне железы. Отмечается экстракапсулярное распространение опухоли, интенсивность сигнала от перипростатической клетчатки изменена. Также определяется метастатическое поражение костей таза и правой бедренной кости (рис. 3 б); при коронарном Т2-взвешенном изображении ИП TSE - участок опухоли в базальных отделах железы слева распространяется на проксимальные отделы левого семенного пузырька. Определяются измененные семенные пузырьки со сниженной интенсивностью сигнала. В костях таза выявляются очаги метастатического поражения (рис. 3 в); при сагиттальном Т1-взвешенном изображении позвоночника, ИП TSE - тела позвонков пояснично-крестцового отдела позвоночника с участками сниженного МР-сигнала (рис. 3 г); при сагиттальном Т2-взвешенном изображении позвоночника, ИП TSЕ - тела позвонков пояснично-крестцового отдела позвоночника с участками сниженного МР-сигнала (рис. 3 д).

а) Метастазы в костях таза и правой бедренной кости.

б) Экстракапсулярное распространение опухоли.

в) Рак предстательной железы.

г) Пояснично-крестцовый отдел позвоночника.

д) Пояснично-крестцовый отдел позвоночника.
Увеличение лимфатических узлов малого таза при ТРУЗИ выявлено не было, при МРТ - определено у 5 (7,7%) пациентов.
Также необходимо отметить, что у 1 (1,5%) пациента при МРТ определялись признаки метастатического поражения костей скелета. Данные изменения были подтверждены результатами радиоизотопного исследования.
По стадии местного распространения, с учетом данных лабораторных методов исследования, анализа гистологического материала, результатов ТРУЗИ с ультразвуковой ангиографией и МРТ: Т2 стадия была установлена в 12 (18%) случаях, стадия Т3 - в 49 (75%)случаях, Т4 - в 4 (6 %) случаях.
На основании проведенного исследования получены следующие показатели информативности для ТРУЗИ с ультразвуковой ангиографией в сопоставлении с МРТ (табл. 3).
| Наименование | ТРУЗИ - B-режим, режим ультразвуковой ангиографии, % | МРТ, % |
|---|---|---|
| Чувствительность: | ||
| участок опухоли | 92 | 72 |
| экстракапсулярное распространение | 84 | 88 |
| вовлечение семенных пузырьков | 87 | 100 |
| Специфичность: | ||
| экстракапсулярное распространение | 95 | 90 |
| вовлечение семенных пузырьков | 95 | 75 |
| Точность: | ||
| экстракапсулярное распространение | 84 | 89 |
| вовлечение семенных пузырьков | 93 | 86 |
Таким образом, при сопоставлении показателей информативности ТРУЗИ с ультразвуковой ангиографией и МРТ в оценке распространенности рака предстательной железы было показано, что чувствительность в выявлении участка измененной паренхимы предстательной железы выше при использовании ТРУЗИ в режиме ультразвуковой ангиографии. Методы ТРУЗИ с ультразвуковой ангиографией и МРТ были сопоставимы в отношении выявления экстракапсулярного распространения: чувствительность 84 и 88%, точность 84 и 89% соответственно. МРТ была намного чувствительнее в определении вовлечения в процесс семенных пузырьков и повышала чувствительность с 87 до 100%. В то же время МРТ позволяет оценить органы мишени при метастазировании процесса - кости таза, пояснично-крестцового отдела позвоночника, попадающих в поле зрения при рутинном исследовании, а также регионарные лимфатические узлы малого таза.
Основываясь на полученных результатах, было выявлено, что ультразвуковая ангиография позволяет более точно дифференцировать изменения в паренхиме предстательной железы (с чувствительностью 92%), в то время как МРТ более четко (чувствительность для экстракапсулярного распространения и инвазии в семенные пузырьки - 88 и 100% соответственно) определяет распространение процесса.
Выводы
Проведенное исследование показало достаточно высокую информативность ТРУЗИ с ультразвуковой ангиографией в диагностике первичного очага и местного распространения рака предстательной железы - на собственную капсулу железы, парапростатическую и параректальную клетчатку, заднюю стенку мочевого пузыря и стенку прямой кишки. Метод ТРУЗИ с ультразвуковой ангиографией более информативен в оценке структуры железы и размеров первичного очага и менее информативен в оценке вовлечения в опухолевый процесс семенных пузырьков, задней стенки прямой кишки, регионарных лимфатических узлов по сравнению с МРТ органов малого таза.
Таким образом, ТРУЗИ с ультразвуковой ангиографией и МРТ в диагностике первичного очага и местного распространения рака предстательной железы являются взаимодополняющими методами лучевой диагностики, применение которых позволяет получить более точное представление о внутренней структуре предстательной железы, размерах и структуре опухоли, распространении опухоли в пределах железы и за капсулу железы.
Литература
- Аксель Е.М., Давыдов М.И. Статистика заболеваемости и смертности от злокачественных новообразований в 2000 г.// Злокачественные новообразования в России и странах СНГ в 2000 г. - М.: РОНЦ им. Н.Н. Блохина РАМН. - 2002. - С. 85-106.
- Аксель Е.М., Матвеев Б.П. Состояние онкоурологической помощи больным в России, 1997 // Клин. онк. - 1999. - Том 1. - N 1. - С. 35-41.
- Александров В.П., Карелин М.И. Рак предстательной железы. - СПб.: Издательский дом СПбМАПО, 2004. - С.55-69.
- Бухаркин Б.В. Рак предстательной железы // Клин. онк. - 1999. - Том 1. - N 1. - С. 10-13.
- Гажонова В.Е., Платицын И.В., Кислякова М.В. Комплексная магнитно.резонансная и ультразвуковая диагностика рака предстательной железы // Кремл. мед. Клин. вест. - 2004, N1. - С. 15-19.
- Гранов А.М., Матякин Г.Г., Зубарев А.В., Чуприк-Малиновская Т.П., Гажонова В.Е., Малофиевская Е.В., Кислякова М.В., Емельянов И.В., Виноградова Н.В. Возможности современных методов лучевой диагностики и лечения рака предстательной железы // Кремл. мед. Клин. вест. - 2004, N1. - С. 9-12.
- Денисов Л.Е., Николаев А.П., Виноградова Н.Н. и др. Рак предстательной железы // Организация ранней диагностики злокачественных новообразований основных локализаций. - М. - 1997. - С. 122-134.
- Зубарев А.В., Гажонова В.Е. Диагностический ультразвук. Уронефрология. - М., 2002. - С. 142-152.
- Матякин Г.Г., Чуприк-Малиновская Т.П., Малофиевская Е.В. Лучевая терапия рака предстательной железы // Кремл. мед. Клин. вест. - 1999. - N 1. - С. 41-44.
- Halpern E.J., Cochlin D.LI, Goldberg B.B. Imaging of the prostate // Martin Dunitz. - 2002. - P. 20-50, 77-99.
- Fleshner N., Rakovitch E., Klotz L. Differences between urologists in the United States and Canada in the approach to prostate cancer // J. Urol. - 2000. - Vol. 163. - N 5. - P.1461-1466.
- Littrup P.J., Bailey S.E. Prostate cancer: the role of transrectal ultrasound and it`s impact on cancer detection and management // The radioligic clinics of North America. - 2000. Jan. - P. 87-114.
- Silverberg E., Boring C.C., Sqires T.S. Cancer statistic // Canc. - 1990. - Vol. 40. - P. 9-26.

УЗ сканер Samsung RS85
Аппарат премиум класса со встроенным искусственным интеллектом, для лечебных учреждений с высокими требованиями к ультразвуковой диагностике.
Публикации по теме
- Использование различных методов лучевой диагностики у детей с патологией почек и мочевыводящих путей - Курзанцева О.М.
- Ультразвуковая и рентгеновская диагностика дивертикулов чашечно-лоханочных систем почек - Буйлов В.М.
- Возможности ТРУЗИ с ультразвуковой ангиографией в оценке местного распространения рака предстательной железы - Кислякова М.В.
- Спонтанный разрыв почки - Аляев Ю.Г.
- Трехмерная УЗ-ангиография в мониторинге консервативного лечения абсцесса предстательной железы - Кислякова М.В.


